Dalla simulazione ingegneristica al supporto clinico: la multifisica entra in oncologia per prevedere l’evoluzione dei tumori e supportare decisioni terapeutiche sempre più personalizzate
Negli ultimi anni la simulazione numerica ha progressivamente esteso il proprio perimetro applicativo ben oltre i confini tradizionali dell’ingegneria industriale. Se settori come l’aerospazio, la meccanica, l’energia o l’automotive hanno da tempo integrato la modellazione multifisica nei propri processi decisionali, oggi un’area fino a poco tempo fa lontana da questi strumenti sta vivendo una rapida trasformazione: l’oncologia clinica.
Un esempio concreto di questo cambiamento lo abbiamo proprio qui in Italia con il lavoro di initiatives for Bio-Materials Behavior (iBMB), spin-off dell’Università della Basilicata, che ha sviluppato CancerMate, una piattaforma di simulazione predittiva per il supporto alle decisioni terapeutiche in ambito oncologico, in particolare per determinati tumori alla mammella da trattare mediante terapie neoadiuvanti. L’obiettivo è ambizioso: utilizzare modelli matematici e computazionali per prevedere l’evoluzione di un tumore e la sua risposta a tali terapie, partendo dai dati clinici reali del singolo paziente, permettendo una personalizzazione delle cure.
Dal modello matematico al “gemello digitale” del tumore
Alla base di CancerMate vi è il concetto di gemello digitale applicato alla medicina: un modello virtuale che replica il comportamento di un sistema reale, in questo caso una lesione tumorale, e che può essere interrogato per simulare scenari futuri. Il tumore non viene descritto come un’entità statica, ma come un sistema dinamico, in continua evoluzione, influenzato da fenomeni biologici, biochimici e terapeutici. Spiega Gianpaolo Ruocco, Professore associato di Fisica tecnica Industriale all’Università degli Studi della Basilicata e fondatore di iBMB: «Il modello prende forma a partire da dati clinici già disponibili nella pratica ospedaliera: immagini diagnostiche, parametri biologici e informazioni sul regime terapeutico. Questi dati alimentano un insieme di equazioni differenziali che descrivono la crescita del tumore, la sua diffusione spaziale e l’effetto dei farmaci somministrati». Il risultato è una simulazione multifisica basata sull’analisi agli elementi finiti, in grado di integrare variabili biochimiche e meccaniche per riprodurre l’evoluzione temporale del volume tumorale, sia nella fase di crescita naturale che in risposta ai trattamenti terapeutici. Il prof. Ruocco tiene a sottolineare: «Dal punto di vista metodologico, l’approccio non introduce nuove equazioni “ad hoc”, ma si inserisce in un filone consolidato di oncologia computazionale, adattando modelli matematici noti a un utilizzo operativo e predittivo. L’innovazione da noi introdotta risiede piuttosto nella capacità di rendere questi modelli utilizzabili in modo sistematico e ripetibile da parte del medico curante, trasformandoli in veri strumenti di supporto alla pratica clinica».

Perché la multifisica è essenziale
«La crescita tumorale e la risposta alle terapie sono fenomeni intrinsecamente multifisici – spiega il prof. Ruocco – Da un lato vi è la proliferazione biologica delle cellule cancerose; dall’altro l’azione chimica dei farmaci, che diffondono nei tessuti e interagiscono con le cellule alterandone i meccanismi di replicazione. Questi processi non sono indipendenti: si influenzano reciprocamente e generano comportamenti non lineari che non possono essere descritti da modelli semplificati». Ecco perché la simulazione multifisica è fondamentale: «Solo tale simulazione permette di affrontare questa complessità» dice il prof. Ruocco. E lo fa integrando in un unico framework:
- la diffusione spaziale della massa tumorale;
- la dinamica temporale della crescita cellulare;
- l’effetto farmacologico delle terapie neoadiuvanti;
- la risposta complessiva del tessuto nel tempo.
In questo contesto, il modello non si limita a “fotografare” una situazione clinica, ma permette di esplorare scenari alternativi: cosa accade se una terapia viene modificata, ad esempio introducendo un diverso principio o regime farmacologico? Qual è l’evoluzione attesa del tumore per quella data paziente? È proprio questa capacità predittiva a rendere l’approccio particolarmente interessante per la comunità clinica. Per un medico curante tutto questo si traduce, ad esempio, in possibilità di valutare effetti di scenari virtuali prima che la paziente venga sottoposta alla terapia e valutare la portata di un intervento chirurgico.
Dalla validazione retrospettiva all’uso prospettico
Il metodo sviluppato da iBMB si basa su un processo in due fasi. In una prima fase, il modello viene calibrato e validato utilizzando coorti di pazienti trattati nel recente passato. I dati retrospettivi consentono di “addestrare” il modello, individuando i parametri (o biomarcatori virtuali) che meglio descrivono la risposta del tumore alle terapie osservate. Una volta validato, il modello può essere applicato in modo prospettico, simulando l’evoluzione di nuovi casi clinici. «In questo scenario – tiene a specificare il prof. Ruocco – la simulazione non sostituisce il giudizio medico ma si propone come strumento di supporto decisionale, in grado di fornire indicazioni quantitative sull’andamento atteso della malattia». Il modello non prende decisioni cliniche, ma fornisce indicatori quantitativi, aiuta a confrontare scenari alternativi di terapia, supporta la scelta tra chirurgia conservativa o mastectomia. Un aspetto particolarmente rilevante è la possibilità di valutare l’efficacia della terapia neoadiuvante prima dell’intervento chirurgico, con potenziali ricadute sia sulla pianificazione dell’intervento sia sulla qualità di vita del paziente oltre che sui costi di cura.
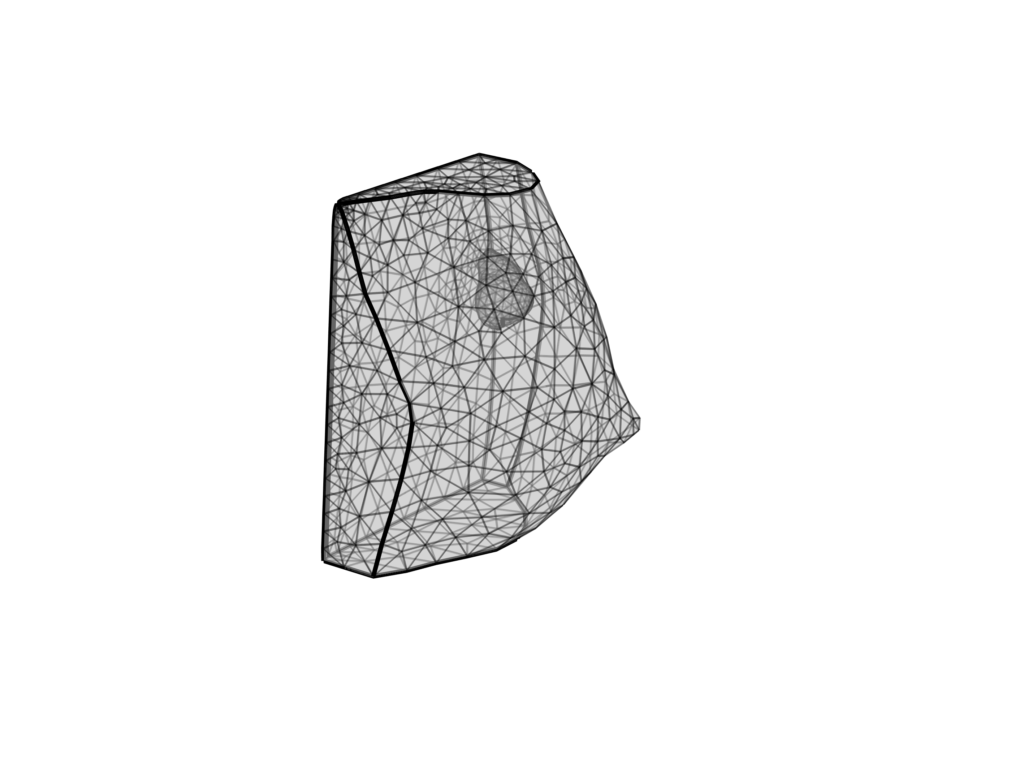
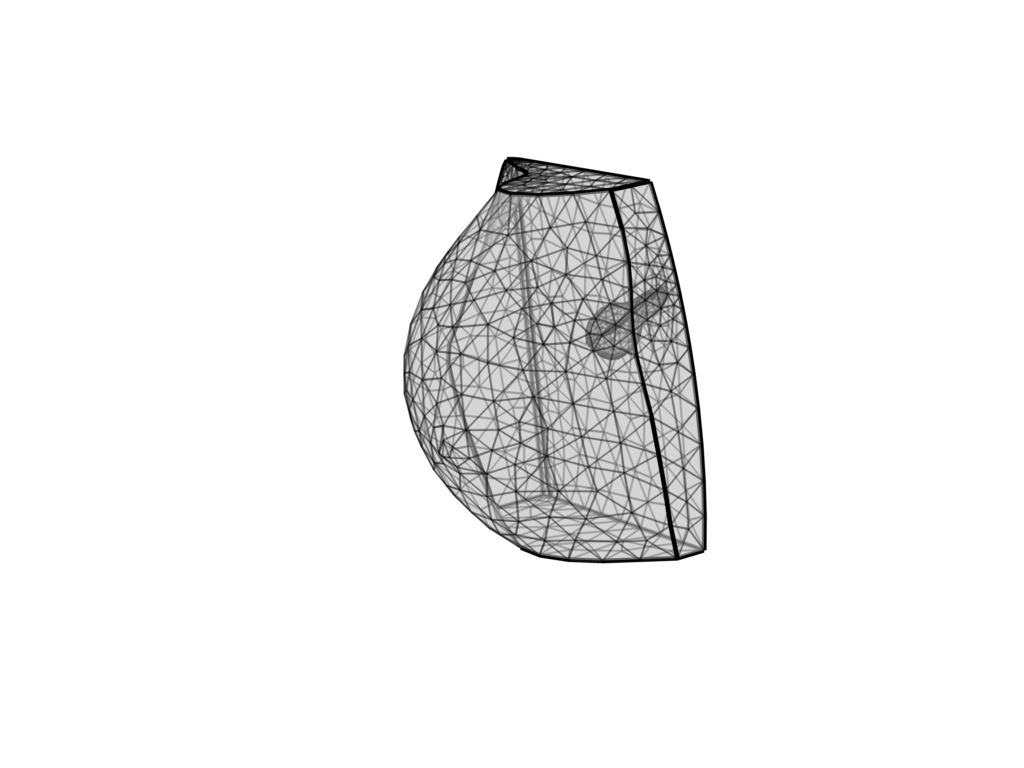
Un cambio di paradigma per l’ingegneria applicata alla medicina
Per il mondo della progettazione industriale, questo caso rappresenta un esempio emblematico di come le competenze e gli strumenti dell’ingegneria multifisica possano trovare applicazione in contesti radicalmente nuovi. La medicina diventa, a tutti gli effetti, un campo di progettazione di sistemi complessi, in cui l’oggetto di studio non è una macchina o un processo produttivo, ma un organismo biologico. La piattaforma CancerMate dimostra come la simulazione non sia più solo uno strumento di verifica a valle, ma possa diventare un elemento attivo nei processi decisionali, aprendo la strada a una progettazione “in-silico” delle terapie, analoga a quella già consolidata in ambito industriale.
Per concludere è fondamentale sottolineare che questo tipo di approccio basato sulla simulazione dell’evoluzione di una lesione al computer serve a ridurre trattamenti inutili, migliorare qualità di vita e ottimizzare le risorse sanitarie. L’obiettivo, cioè, non è “curare col computer”, ma anticipare chi risponderà e chi no e di conseguenza adeguare le cure al caso specifico. Un passo avanti fondamentale per medici e pazienti.
Perché la simulazione multifisica in oncologia
Nel contesto dello sviluppo di modelli multifisici complessi come quelli utilizzati in oncologia computazionale, la scelta dell’ambiente di simulazione assume un ruolo chiave. Per la analisi descritte in questo testo è stato usato COMSOL Multiphysics che offre alcune caratteristiche particolarmente rilevanti per questo tipo di applicazioni:
- Integrazione nativa di fenomeni multipli: la piattaforma consente di accoppiare in modo diretto modelli di diffusione, reazione e trasporto, facilitando la rappresentazione di processi biologici e biochimici interdipendenti all’interno di un unico framework.
- Flessibilità nella definizione delle equazioni: l’approccio equation-based permette di implementare modelli matematici personalizzati, senza essere vincolati a fisiche predefinite, aspetto essenziale nella modellazione di sistemi biologici complessi.
- Passaggio dal modello all’applicazione: la possibilità di trasformare i modelli in applicazioni dedicate consente di rendere la simulazione accessibile anche a utenti non specialisti di calcolo numerico, come medici e ricercatori clinici.
- Riduzione della curva di apprendimento: l’ambiente grafico integrato facilita la gestione di modelli multifisici complessi, riducendo i tempi di sviluppo e favorendo l’interazione tra ingegneri, informatici e personale medico.
In questo senso, COMSOL si configura non solo come strumento di calcolo, ma come ponte tecnologico tra ingegneria e medicina, abilitandoabilitando nuovi scenari applicativi per la simulazione multifisica in ambito clinico.




